Chondrome rodens
Sommaire
- Le chondrome rodens est une tumeur rare chez le Chien, atteignant plus volontiers les os du crâne.
- Nous décrivons ici le diagnostic et le traitement chirurgical d’un chondrome rodens survenu chez un berger malinois de 9 ans.
- Il est important d’intervenir rapidement sur ces tumeurs afin de pouvoir réaliser une exérèse aussi complète que possible.
Auteurs : Drs. A. Gautherot et S. Etchepareborde 19-06-2013
Centre Hospitalier Vétérinaire des Cordeliers, 29 avenue du Maréchal Joffre, 77100 Meaux.
E-mail : agautherot@chvcordeliers.com
Cet article a été publié dans : L’Essentiel (2013) : p 86-88
Chondrome rodens
À propos d’un cas clinique
Anamnèse
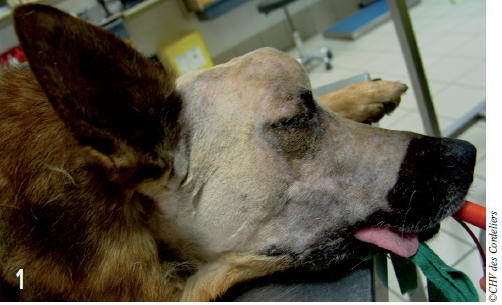
Un chien malinois mâle de 9 ans est référé en consultation pour l’exploration d’une masse ferme sur le haut du crâne (photo 1).
Présente depuis des mois, elle a subitement grossi en 3 semaines. Une biopsie réalisée la semaine avant la consultation par le vétérinaire traitant a mis en évidence un chondrome multilobulaire. L’examen général est par ailleurs normal. La palpation de la masse n’est pas douloureuse.
Examens complémentaires
Un bilan sanguin complet est réalisé (NFS, biochimie, ionogramme, temps de coagulation) et ne montre aucune anomalie.
Un bilan tomodensitométrique est entrepris.
Le crâne et le thorax sont examinés pour déterminer respectivement l’envahissement local du calvarium et la présence de métastases pulmonaires.
- Rostralement, la masse recouvre les sinus frontaux dorsalement et les envahit (photo 2).
- Caudalement, le tissu hyperdense après l’injection de produit de contraste s’étend jusqu’au milieu de la crête occipitale.
- Latéralement, la masse déborde de façon plus importante du côté gauche avec un envahissement du processus zygomatique de l’os frontal et s’étend 1 cm en arrière de l’œil (photo 3).

Photo 2 : Aspect tomodensitométrique de la masse : notez l’envahissement des sinus frontaux (étoiles) et la latéralisation à gauche (flèche).
Aucune compression du cerveau n’est visible au scanner.
Les images thoraciques ne mettent pas en évidence de métastase à distance.
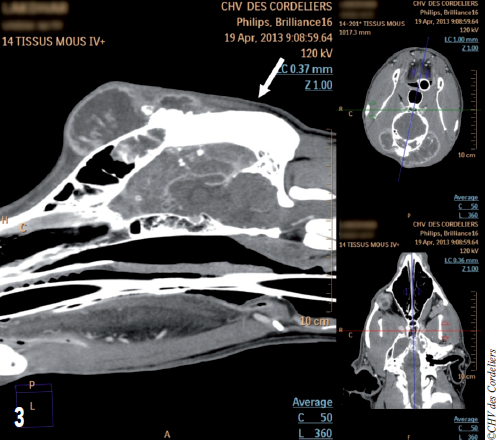
Photo 3 : Aspect tomodensitométrique de la masse en vue sagittale : la masse s’étend très caudalement (flèche).
Traitement
Un traitement chirurgical est considéré compte tenu de la vitesse d’accroissement de la tumeur et du risque de compression cérébrale.
L’animal est préparé pour la chirurgie et positionné en décubitus sternal (photo 4).
Une crâniotomie est réalisée en prenant des marges de 5 à 10 mm autour de la masse (photo 5).
Les sinus frontaux sont ouverts puis les os frontaux, pariétaux et occipital sont coupés pour permettre la résection de la tumeur (photos 6a et 6b).
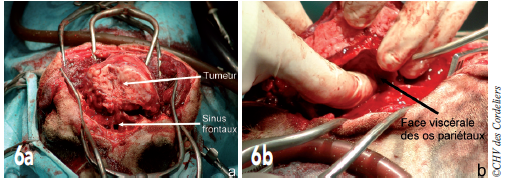
Photos 6a et 6b : Les sinus frontaux et os frontaux, pariétaux et occipital ont été découpés à la fraise et à la scie oscillante (a), permettant la résection en bloc de la tumeur (b).
Afin de prétendre à des marges saines, le processus zygomatique de l’os frontal gauche est retiré. Le cerveau est alors exposé (photo 7).
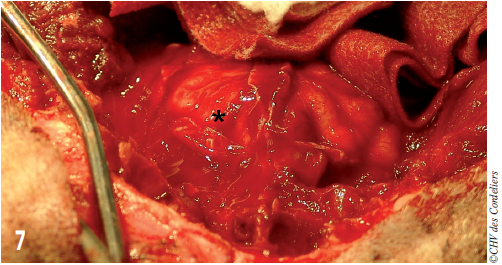
Photo 7 : L’encéphale est exposé ; L’hémisphère droit est ici recouvert des méninges (étoile) ; elles seront réséquées pour analyse anatomo-pathologiques (marges profondes).
L’hémostase est réalisée grâce à des compresses de collagène (photo 8).
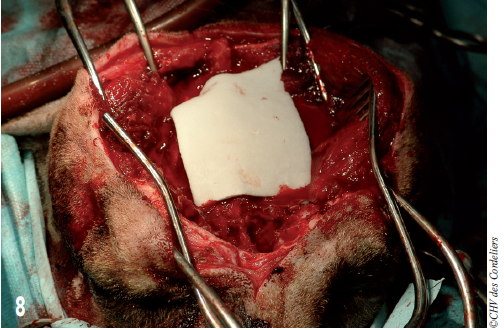
Photo 8 : Le cerveau est temporairement couvert par une compresse de collagène (Pangen®) afin d’assurer l’hémostase.
Une greffe de fascia temporal est utilisée pour recouvrir le cerveau et fixée aux méninges des bords de la crâniotomie (photo 9).
Les muscles temporaux sont refermés puis le tissu sous-cutané et la peau sont suturés classiquement.
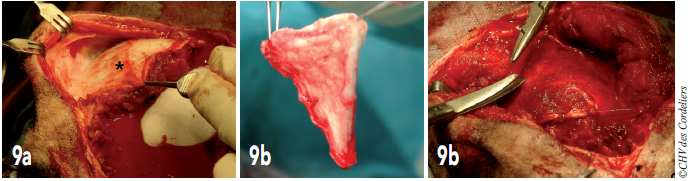
Photos 9a—c : Le fascia temporal (étoile) est disséqué (a), isolé (b) puis suturé pour recouvrir l’encéphale, sa face superficielle étant placée contre le cerveau (c)
Une acquisition scanner est réalisée avant de placer l’animal en réveil (photo 10).

Photos 10a et 10b : Images tomodensitométriques en post-opératoire immédiat en vue sagittale (a) et en vue frontale (b)
L’animal est gardé sous sédation pendant 6 heures avec une perfusion de chlorhydrate de Fentanyl (dose de charge à 2 μg / kg / h IV) pour permettre un réveil progressif et calme.
Suivi post-opératoire
L’intervention n’a « malheureusement » pas modifié le caractère agressif du chien qui montrait déjà les dents quelques heures après la chirurgie (photo 11).
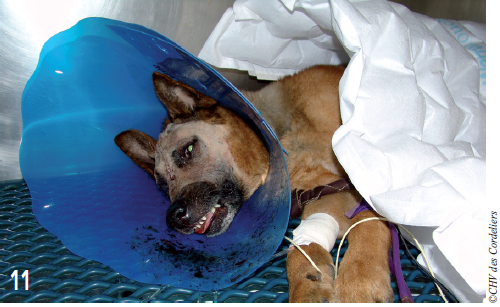
Photo 11 – Le comportement de l’animal en hospitalisation ne permet pas de réaliser de soin sans anesthésie générale.
Compte-tenu de son agressivité et d’une très bonne récupération, l’animal est sorti après 24 heures d’hospitalisation, en marchant.
Une antibiothérapie est instaurée (amoxicilline/acide clavulanique 20 mg / kg BID) pour 3 semaines.
L’antalgie est assurée par du carprofène (4 mg / kg PO SID), du tramadol (5 mg / kg PO TID) et de la gabapentine (2 mg / kg TID).
Au contrôle téléphonique à 1 mois, les propriétaires décrivent un retour à une activité normale sans trouble neurologique rapporté.
L’examen histopathologique de la tumeur confirme le chondrome rodens et souligne la présence d’éléments en faveur d’une transformation maligne vers un chondrosarcome multilobulaire (perte focale d’organisation lobulaire, plages hémorragiques, index mitotique modéré à élevé). Les marges profondes sont saines mais la tumeur est en contact étroit avec les marges latérales. Le risque de récidive locale n’est donc pas négligeable.
Discussion
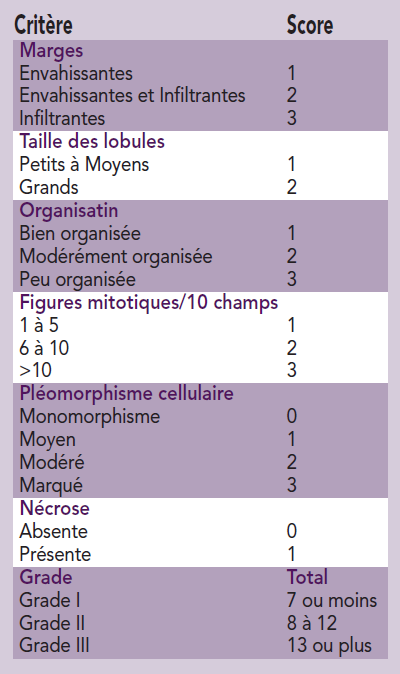
Tableau de grades histologiques basé sur le système établit par Straw, et al1
Également nommé chondrome -, ostéome -, ostéochondrome -, ou ostéochondrosarcome multilobulaire, le chondrome rodens est une tumeur primaire rare des os plats, principalement du crâne (calvarium, mandibule, maxillaire)1.
Bien que des cas aient été rapportés sur des chiens jeunes ou de race de petit format2, ce type de tumeur est plus fréquent chez des chiens d’âge moyen à vieux et de taille moyenne à grande comme dans le cas décrit ici. En revanche, aucune prédisposition raciale ou sexuelle n’est mise en évidence1.
Classiquement, le motif de consultation est la présence d’une masse ferme et adhérente au crâne. Selon la localisation ou le degré d’envahissement de la tumeur, des symptômes neurologiques3 ou oculaires4 peuvent également être observés.
De croissance lente, la tumeur est localement très invasive et présente un haut degré de récidive locale (près de 50 %)1 avec un potentiel métastatique modéré, pulmonaire en général.
L’examen tomodensitométrique permet d’obtenir des images typiques (photos 2 et 3) d’une masse granuleuse et non homogène envahissant le calvarium5.
L’analyse histopathologique permet d’établir le diagnostic de chondrome rodens, le différentiel incluant l’ostéosarcome, l’hémangiosarcome, le fibrosarcome et le chondrosarcome.
Dans notre cas, une biopsie a d’abord été réalisée puis un examen tomodensitométrique a permis de déterminer l’envahissement de la masse (pour en définir les marges d’exérèse) et de réaliser le bilan d’extension à distance. Le grade histologique (sur base du système établit par Straw, et al.1 (tableau)) constitue un facteur de pronostic. Il permet notamment de déterminer les médianes de survie et du temps avant récidive locale.
Dans notre cas particulier, la tumeur est de grade II. La médiane de survie attendue est donc de 520 jours1.
Une résection chirurgicale agressive constitue le traitement de choix. L’obtention de marges saines, compliquée par la présence des structures vitales risquant d’être lésées, réduit drastiquement les risques de récidives locales. Dans le cas décrit plus haut, les marges latérales de la pièce d’exérèse sont en étroit contact avec la tumeur, augmentant significativement le risque de récidive.
La cranioplastie reconstructrice est souhaitable lorsque le défect osseux est important mais la présence d’un volumineux implant est corrélé à un risque infectieux, en particulier lorsque le sinus frontal est exposé4. Plusieurs techniques sont décrites pour refermer le calvarium4.
Dans notre cas, le choix s’est porté sur une greffe du fascia du muscle temporal. L’utilisation d’allogreffe osseuse2, de prothèse en polyméthyl-méthacrylate2, 6 ou de greffe de sous-muqueuse
intestinale de porc7 sont également rapportées.
Les chondromes multilobulaires sont donc principalement des tumeurs malignes d’agressivité locale. Le diagnostic précoce est important puisqu’il améliore les chances de pouvoir complètement retirer la masse chirurgicalement.
La chirurgie comporte un risque hémorragique important et les animaux nécessitent dans la majorité des cas des soins intensifs pendant plusieurs jours.
Bibliographie
|

