La coproscopie chez le Chien et le Chat
Sommaire
- La coproscopie est un examen abordable car peu onéreux, facile et rapide. Bien que simple, elle conserve tout son intérêt comme outil de diagnostic ou de dépistage tant à l’échelle de l’individu que de la collectivité.
Auteur : Dr. E. Rattez 01-11-2013 Centre Hospitalier Vétérinaire des Cordeliers, 29 avenue du Maréchal Joffre, 77100 Meaux. E-mail : erattez@chvcordeliers.com Mots clefs : Cet article a été publié dans : PratiqueVet (2011) 46 : p 33-37
Objectifs pédagogiques
- Savoir quand et comment faire une coproscopie chez le Chien et le Chat.
- Savoir interpréter le résultat d’une coproscopie et quand recourir à un autre examen.
Crédit de formation continue
La lecture de cet article ouvre droit à 0,05 CFC. La déclaration de lecture, individuelle et volontaire, est à effectuer auprès du CNVFCC.
La coproscopie chez le Chien et le Chat : toujours un examen d’actualité ?
À l’heure des examens complémentaires nécessitant de plus en plus de technicité, que pouvons nous attendre de la coproscopie en pratique quotidienne ?
La coproscopie est un examen rapide qui peut orienter le diagnostic du praticien. Réalisable au chevet du patient, il nécessite souvent le recours à un laboratoire vétérinaire.
Cependant même bien conduite, la coproscopie présente des limites qu’il faut connaître pour savoir quand y associer ou y préférer un autre examen complémentaire plus pertinent.
Qu’est ce que la coproscopie ? Est-ce différent d’un examen de selles ?
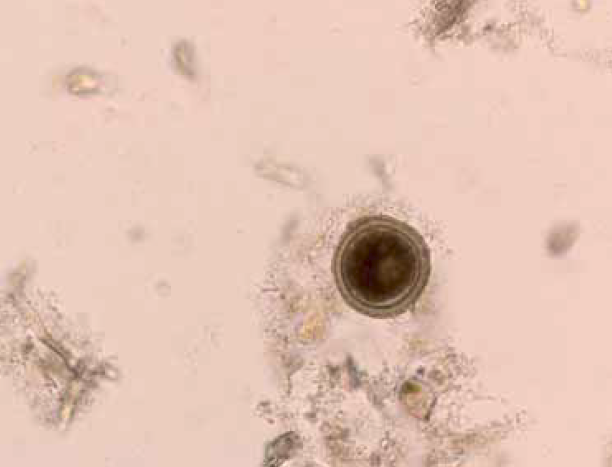
La coproscopie est l’examen des matières fécales, elle comprend un examen macroscopique (consistance, présence de sang, glaires, ascarides, segments ovigères lors de taeniasis…) et un examen microscopique [1–3]. L’objectif est la reconnaissance d’éléments parasitaires pathogènes dans l’espèce étudiée (œufs, larves, ookystes…). Elle appartient à l’examen de selles.
Celui-ci consiste, en plus d’une coproscopie, à effectuer différents dosages et à rechercher des agents pathogènes bactériens ou viraux normalement absents (coproculture, PCR, immunologie…)[2].
Dans quels cas recourir à une coproscopie ?
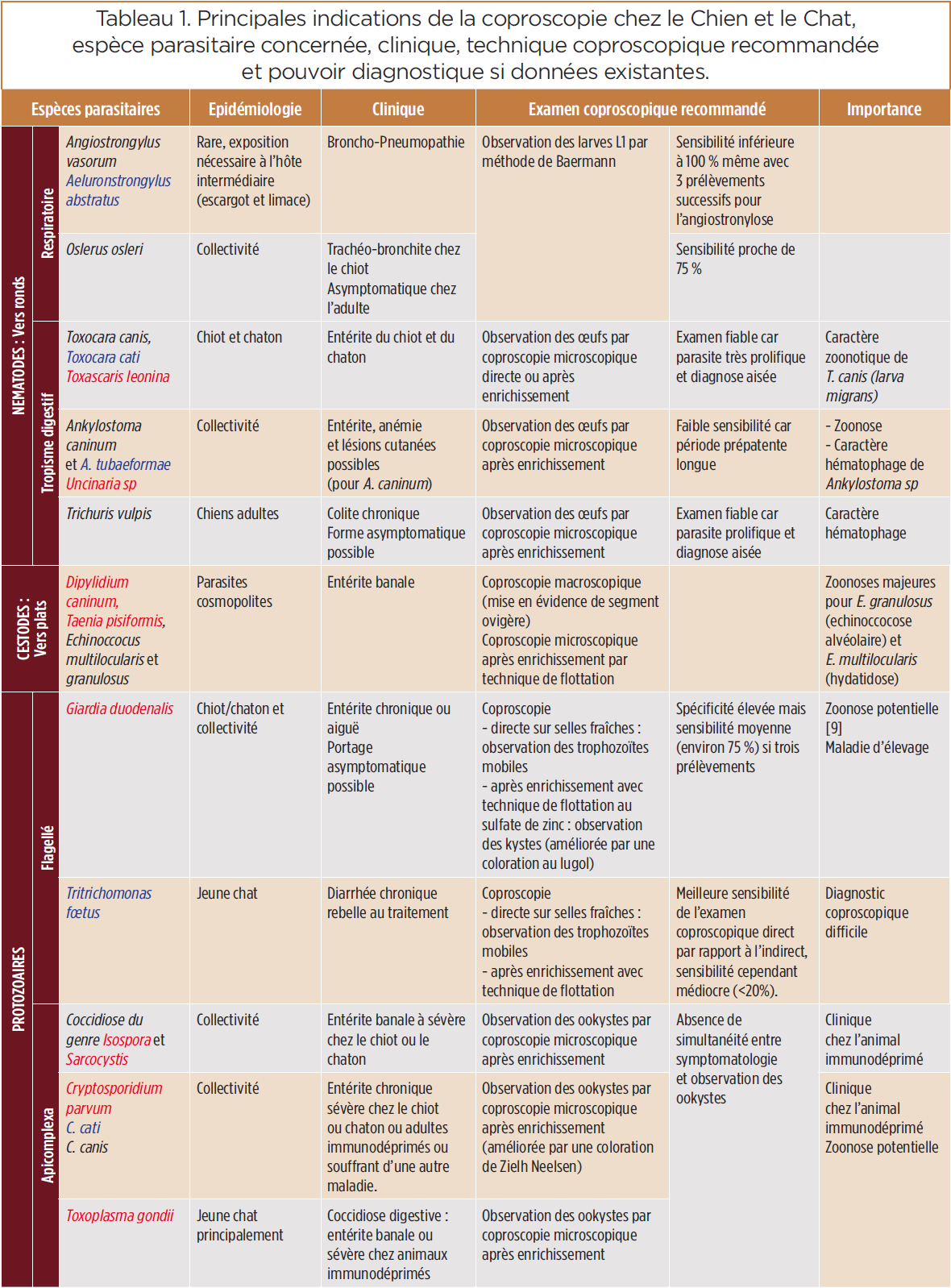
La coproscopie a surtout pour but de dépister (porteur asymptomatique) ou de confirmer une suspicion de parasitose à élimination fécale (Tableau 1). C’est un examen simple, peu coûteux, et rapide.
Mise en évidence d’une cause parasitaire dans l’exploration de signes digestifs.
L’une des indications est la mise en évidence d’une cause parasitaire dans l’exploration de signes digestifs, quelles qu’en soient la localisation, la nature, l’ancienneté ceci, à l’échelle de l’individu ou de la collectivité (chenil/chatterie ou élevage).
Malgré une symptomatologie plus discrète que chez le chiot ou le chaton, une origine parasitaire ne doit pas être négligée chez l’adulte, en particulier lors de gastro-entérite chronique ou d’amaigrissement sans signe digestif [4].
Une coproscopie peut être indiquée pour suivre l’efficacité d’un traitement en cours.

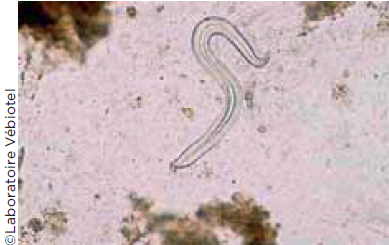
Photo 1
Larves L1 d’Angiostrongylus vasorum, x 10.
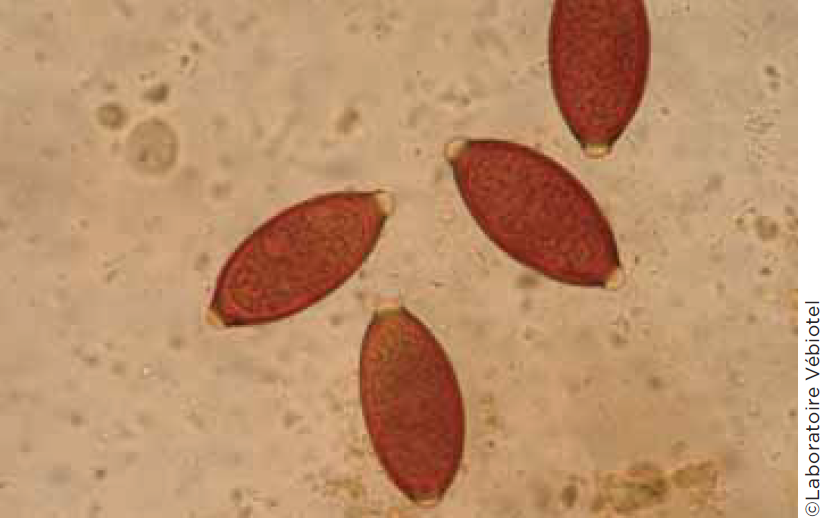
Photo 2
Œufs de Trichuris vulpis, x 40
Dépistage des porteurs asymptomatiques
La coproscopie est utile au dépistage des porteurs asymptomatiques. Au sein d’une collectivité, il est possible de contrôler le statut d’un arrivant et d’établir un programme de prophylaxie.
Le dépistage à l’échelle individuelle reste plus rare. Il se justifie pourtant en raison du potentiel zoonotique de certaines maladies (larva migrans lors de toxocarose).
Exploration d’une affection respiratoire tussigène et/ou dyspnéique
Étant donné qu’une partie du cycle de parasites trachéo-bronchiques (Angiostrongylus vasorum chez le Chien (Photo 1) ou Aelurostrongylus abstratus) comprend une localisation digestive, une coproscopie est indiquée dans l’exploration d’une affection respiratoire tussigène et/ou dyspnéique.
Exploration d’une anémie ferriprive
Enfin, une indication de coproscopie est l’exploration d’une anémie ferriprive éventuellement secondaire à une infestation par des parasites hématophages (Trichuris vulpis chez le Chien (Photo 2)…).
Quelles sont les règles à respecter pour faire une coproscopie ?
L a quantité prélevée doit être suffisante (2 à 5 g et 10 g pour la technique de Baermann). Plus les selles sont liquides, plus la quantité doit être importante.
Les selles analysées doivent être fraîches et non souillées (éviter les excréments prélevés au sol, potentiellement contaminés par des Nématodes libres). L’idéal est de récolter les fèces en intrarectal ou immédiatement après la défécation.
Multiplier les prélèvements
L’élimination de certains parasites dans les selles étant intermittente et/ou en faible quantité, il est recommandé de multiplier les prélèvements.
La réalisation de trois prélèvements consécutifs est conseillée pour l’angiostrongylose, l’aeluronstrongylose et la giardiose [5–7].
Il est conseillé de faire l’envoi groupé au laboratoire des différents prélèvements non mélangés.
Si l’analyse immédiate est impossible, les selles sont gardées plusieurs jours dans un pot propre, à l’obscurité et au frais (+4 °C). Cela permet l’arrêt du cycle de la majorité des parasites ainsi que leur conservation. Giardia duodenalis, Angiostrongylus vasorum et Aelurostrongylus abstratus étant fragiles, l’analyse dans les meilleurs délais est recommandée.
La suspicion clinique est nécessaire au choix de la technique de coproscopie
Les réalisations conjointes d’une coproscopie macroscopique et microscopique sont systématiques. Plusieurs techniques microscopiques existent (Encadré 1).
Le choix entre ces méthodes est dicté par la suspicion clinique. Si l’examen est réalisé en laboratoire, l’hypothèse diagnostique doit clairement être énoncée [5].
| Encadré 1 : Les techniques de coproscopie miscroscopique |
|
Par exemple, lors de suspicion de parasitose trachéo-bronchique, la technique de Baermann sera privilégiée [6,7].
En noir, les parasites spécifiques au Chien, en bleu ceux spécifiques du Chat et en rouge ceux du Chien et du Chat.
Est-il possible de réaliser soi-même une coproscopie ?
L ’examen macroscopique est aisé et informatif. Cette étape peut être réalisée à la clinique. Pour la coproscopie microscopique, l’examen direct est également abordable : facile à réaliser, il ne nécessite aucun matériel spécifique.
La lecture est cependant gênée par les débris d’aliments. Cette technique est à réserver aux parasites prolifiques et pour lesquels la diagnose ne peut être sujette à caution. T. canis, T. leonina et T. cati répondent à ses critères (Photo 3) [2,3].
Les autres techniques de coproscopie microscopique requièrent un matériel spécifique, du temps, la manipulation de solutions toxiques et des connaissances pointues en parasitologie.
Certains kits de flottation existent et sont abordables en clinique (kit Ovassay®) ; il n’en reste pas moins que la diagnose parasitaire est une discipline complexe.
Nous conseillons donc de réserver cette partie de la coproscopie au laboratoire spécialisé [2].
Comment interpréter le résultat d’une coproscopie ?
L’interprétation d’une coproscopie est à faire en fonction des faux-positifs et faux-négatifs.

Photo 4
Contamination de selles par des poils de pêche pouvant être confondus avec une larve d’Angiostrongylus vasorum, x 40.
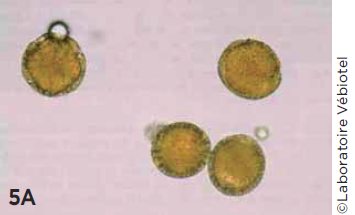
Photo 5a
Photos 5A et 5B.
Pollen de troène (A) pouvant être confondu avec des oeufs de Taenia saginata (B),
x 40.
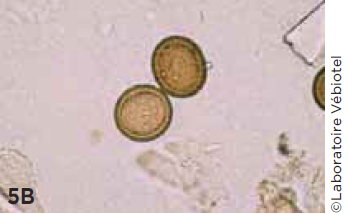
Photo 5b
Les faux positifs en coproscopie
Ils sont obtenus suite à l’ingestion passive d’éléments parasitaires (pseudoparasitisme) ou contamination du prélèvement (Photos 3 et 4).
Les faux négatifs en coproscopie
Ils sont dus à une technique inappropriée, erreur pré-analytique (mauvaise conservation…), élimination irrégulière, forme de dissémination insuffisante (parasite peu prolifique) voire absente (période pré-patente).
Interprétation d’un résultat positif
Face à un résultat positif, un traitement est à mettre en place et ce quel que soit le nombre d’éléments parasitaires observés car il n’existe aucun lien entre la charge parasitaire fécale et l’intensité de la maladie.
Lors de charge importante, on peut bien sûr conclure à un parasitisme élevé, mais l’inverse n’est pas forcément vrai.
Le cas de la coccidiose peut faire exception. En effet, la mise en évidence d’ookystes de coccidies chez l’adulte non immunodéprimé n’étant pas anormal, elle ne conduira pas systématiquement à une thérapie [3].
Interprétation d’un résultat négatif
Lors de résultat négatif et de suspicion clinique élevée, le recours à d’autres examens complémentaires, s’ils existent, est alors nécessaire.
La coproscopie a-t-elle des limites ?
Même bien conduite, la coproscopie peut ne pas confirmer notre suspicion.
Cas de l’angiostrongylose
Le diagnostic d’une broncho-pneumopathie due à l’angiostrongylose repose sur la mise en évidence de larves L1 (Photo 1) soit dans les selles, soit dans le liquide de lavage bronchoalvéolaire.
Aucune de ces deux techniques n’ayant une sensibilité parfaite (absence de données exactes), le recours à la coproscopie, simple et non risquée, se justifie en première intention.
Malgré la réalisation de prélèvements successifs, il est fréquent que cet examen soit négatif, un lavage broncho-alvéolaire doit alors être entrepris [6,7].
Pour certaines parasitoses, de nouvelles techniques plus performantes ou moins contraignantes que la coproscopie sont en développement ou déjà accessibles en pratique. Cest le cas de la giardiose (Encadré 2 et photo 6).
| Encadré 2 : La giardiose canine et féline [5,8] |
À noter que ce test peut rester positif plusieurs semaines après l’élimination du parasite, il n’est donc pas recommandé lors du suivi de traitement. |
Cas de la giardiose
Des techniques ELISA ou PCR sont également à l’étude pour l’angiostrongylose et certaines coccidioses notamment…
Même si la coproscopie est un examen simple, il garde, à ce jour, encore tout son intérêt. D’autres tests aux indications plus restreintes, mais parfois au pouvoir diagnostic plus performant sont en cours de développement et pourraient détrôner la coproscopie.
Mémo
|
RemerciementsAu Docteur Christine Médaille, du Laboratoire Vébiotel |
À lire…
|