Dilatation de l’estomac
Gastropexie par laparoscopie
La gastropexie est la seule méthode communément admise pour prévenir le syndrome de dilatation-torsion de l’estomac (SDTE). Classiquement effectuée par laparotomie, la gastropexie mini-invasive est privilégiée depuis quelques années.
Nous présentons ici un cas de dilatation de l’estomac et de la réalisation d’une gastropexie assistée par laparoscopie après réanimation médicale d’urgence.
Auteurs: Drs. Bille, Poyart et Libermann. 24-09-2010
Centre Hospitalier Vétérinaire des Cordeliers, 29 avenue du Maréchal Joffre, 77100 Meaux.
E-mail: cbille@chvcordeliers.com et slibermann@chvcordeliers.com
Cet article a été publié dans : L’Essentiel 186: p 20 – 26
Un chien de race bouvier des Flandres est référé au service d’urgence pour suspicion de SDTE. L’animal présente des efforts de vomissements infructueux, un ptyalisme et un abdomen distendu depuis 2 heures. L’examen clinique montre un animal agité, en polypnée et tachycardie avec un rythme cardiaque régulier et un pouls fémoral synchrone et un temps de recoloration capillaire (TRC) de 1 seconde. Une douleur abdominale est présente. Elle se manifeste par une contraction de la sangle abdominale associée à une plainte lors de la palpation. Un tympanisme abdominal est identifié.
Compte tenu de l’anamnèse, des commémoratifs et de l’examen clinique le diagnostic est celui d’un syndrome dilatation-torsion de l’estomac. L’animal présente un état de choc compensé. Il est supposé qu’une hypovolémie relative est la composante principale de l’état de choc. Le traitement de l’état de choc, qui traduit un déficit énergétique à l’échelle cellulaire, est prioritaire. Des manœuvres de réanimation sont effectuées sans délai.
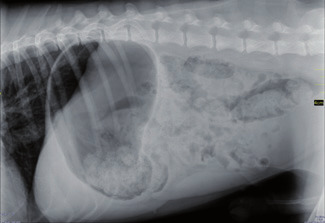
Photo 1a - Radiographie abdominale du patient : dilatation de l’estomac.
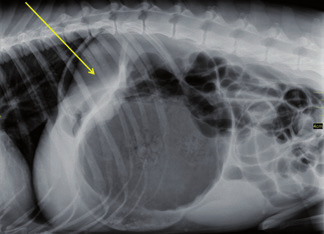
Photo 1b - En comparaison avec une radiographie abdominale montrant une torsion de l’estomac, noter la position dorsale du pylore.
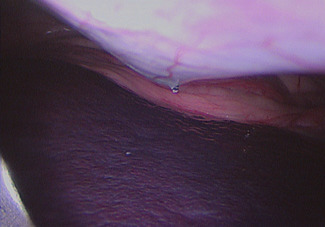
Photo 2 - Visualisation de la rate, noter l’estomac en position physiologique en arrière plan
Réanimation médicale d’urgence
Si l’administration d’O2 est le meilleur moyen de lutter contre le déficit énergétique l’état d’agitation de l’animal n’a pas permis la pose de lunettes à oxygène.
Un remplissage vasculaire rapide est effectué : 3 bolus itératifs de 20 ml/kg de Ringer Lactate sont administrés le plus vite possible (environ 10 minutes). La réponse à la fluidothérapie est évaluée cliniquement par une diminution de la fréquence cardiaque et de la fréquence respiratoire associées à un allongement du TRC (2 secondes). Cette évolution tend à confirmer l’hypothèse d’un état de choc dont la composante principale est l’hypovolémie. La douleur abdominale est traitée par des bolus de morphine (0,2 mg/kg, IV). Deux bolus sont nécessaires pour soulager la douleur. L’administration de morphine a aussi pour effet de tranquilliser le patient.
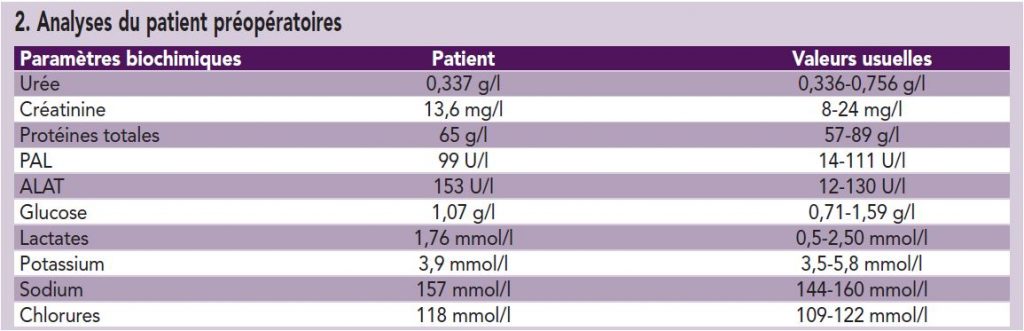
Le sang collecté lors de la pose des cathéters est analysé après la mise en oeuvre de la réanimation. Les résultats des analyses sanguines sont compris dans les intervalles de valeurs usuelles. Ils sont répertoriés dans le tableau 2.
Des radiographies de l’abdomen mettent en évidence une dilatation de l’estomac sans signes de torsion (Photos 1a et 1b). L’hypothèse de dilatation de l’estomac est confirmée.
Une anesthésie générale est effectuée afin de pratiquer un sondage gastrique. De l’acépromazine (20 μg/kg, IV), associée à la morphine déjà administrée, permettent d’obtenir une prémédication. L’induction anesthésique est effectuée avec du propofol (Rapinovet®, IV, à effet, dose effective, environ 2,5 mg/kg) et le maintien avec de l’isoflurane dilué dans de l’oxygène.
L’estomac est vidangé. L’objectif est alors de poursuivre la réanimation médicale en évitant les récidives de dilatation gastrique. Pour ce faire, une sonde de pharyngostomie, plus petite que la sonde de vidange gastrique est mise en place à demeure. Après une préparation aseptique succincte, la peau est incisée caudo-médialement à l’angle mandibulaire gauche. Les tissus sont tunnélisés de manière à établir une communication entre le pharynx et la plaie et le passage
de la sonde.
La sonde est fixée à l’aide d’un laçage chinois.
Les paramètres vitaux (fréquence cardiaque, fréquence respiratoire, température et douleur) sont évalués en continu. La fluidothérapie est maintenue par une perfusion intraveineuse de Ringer Lactate à un débit de 50 ml/kg/24 h. Si une modification de ces paramètres laisse supposer une récidive de l’état de choc, des bolus itératifs de 10 ml/kg de Ringer Lactate sont administrés. La douleur est évaluée et traitée par des bolus intraveineux de 0,2 mg/kg de morphine toutes les 4 heures. Si une douleur est identifiée, la fréquence d’administration de la morphine est augmentée. Une antibiothérapie est instaurée (céphalexine, Rilexine®, 15 mg/kg IV toutes les 8 heures).
Après 10 heures de réanimation, l’état clinique de l’animal étant jugé satisfaisant, une gastropexie laparoscopique est entreprise.
Technique chirurgicale
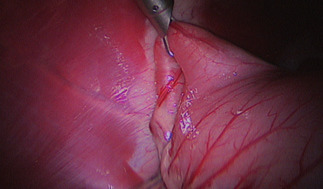
Photo 3 - Le pylore est saisi par la pince à préhension et ramené sur le site d’insertion de la canule.
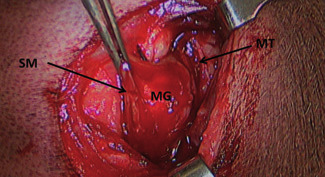
Photo 4 - Séparation de la séromusculeuse (SM) de la muqueuse gastrique (MG). MT= muscle transverse.
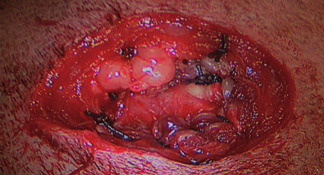
Photo 5 - Suture de la séromusculeuse au muscle transverse, aspect final.
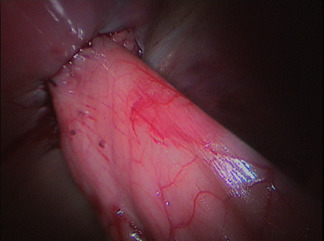
Photo 6 - Aspect de la pexie, vue laparoscopique.
Le matériel se compose d’une colonne de cœlioscopie comprenant un insufflateur CO2, une source de lumière froide, une caméra et une optique, un écran moniteur et 2 trocarts qui serviront de portes optique et instrumentale. L’animal est placé en décubitus dorsal, un peu en rotation
à gauche afin de dégager le flanc droit, et préparé de manière aseptique.
Une première canule est placée à 2-3 cm en arrière de l’ombilic après incision de la peau, des tissus sous-cutanés et de la ligne blanche (technique de l’open-coeliochirurgie). Elle permet l’insertion de l’optique et l’insufflation de la cavité abdominale avec du gaz carbonique à une pression de 12 mm Hg afin d’aménager un espace de travail entre les viscères et la paroi. L’omentum étant fixé sur la grande courbure de l’estomac, il permet donc de déterminer si un volvulus est présent de manière simple : s’il recouvre totalement l’estomac la torsion est certaine. Dans notre cas il est en position physiologique ce qui confirme l’absence
de modification de son axe. La rate est visualisée et ne présente aucune anomalie (Photo 2).
Une canule instrumentale est placée à 2-3 cm de la 13e côte et à 3-4 cm à droite de la ligne blanche, en regard de la position du pylore. Une pince de Babcock est introduite par cette porte et utilisée pour la préhension de l’antre pylorique, entre la grande et la petite courbure de l’estomac.
Celle-ci est amenée en contact avec la paroi abdominale sous contrôle visuel après désufflation de l’abdomen (Photo 3).
La canule instrumentale est retirée et l’incision du site d’insertion de la canule est prolongée de 3 cm parallèlement à la dernière côte. Deux points de soutien comprenant la paroi de l’estomac et le muscle transverse sont placés aux extrémités de la plaie. Une incision intéressant la couche séromusculaire de la paroi stomacale est réalisée et une dissection mousse de 1 cm de large permet de la séparer de la muqueuse gastrique (Photo 4).
Les deux lambeaux séromusculaires sont suturés au muscle transverse à l’aide de deux surjets simples (fil résorbable synthétique déc. 4, type polyglactin 910) (Photo 5).
Les muscles oblique interne, oblique externe, le tissu sous-cutané et la peau sont ensuite suturés de manière usuelle. Une nouvelle insufflation permet de vérifier la qualité de la pexie et l’axe physiologique de l’estomac (Photo 6).
Un monitoring postopératoire est instauré pendant 48 heures (ECG, saturation en O2, T°, évaluation de la douleur).
Les électrocardiogrammes ont montré de rares extrasystoles ventriculaires (moins de 5 par minute) qui se sont résolues sans traitement. L’animal s’est réalimenté le lendemain de la chirurgie. Il est rendu à ses propriétaires 72 h postopératoires avec une prescription de céphalexine (Rilexine® à 15 mg/kg PO toutes les 12 heures) pendant 15 jours et de carprofène (Rimadyl® à 4 mg/kg PO une fois par jour). Lors du contrôle à 1 mois, l’animal est en bon état
général. Une lésion inflammatoire (sérome, complication usuelle de ce type de pexie laparoscopique) est mise en évidence en regard de la plaie de pexie qui a rétrocédé sans traitement.
Discussion
Le SDTE est une affection à laquelle les chiens de grand ou très grand format (Irish wolfhound, dogue allemand, St Bernard…) sont prédisposés. Les origines de ce syndrome sont encore mal connues. Le taux de mortalité est important. Il est compris, selon les auteurs, entre 13,5 % et 80 %.
Le pronostic est plus réservé en cas de volvulus que lors de dilatation simple1. La pexie de l’estomac est la seule technique recommandée permettant d’éviter sa torsion ou ses récidives. En effet un traitement médical uniquement montre une récidive de 76 % et un taux de mortalité de
80 %1.
Si la nécessité d’avoir recours à un geste chirurgical est indiscutable il n’existe pas de consensus sur le moment le plus opportun pour l’effectuer. Certains le réalisent en urgence alors que d’autres recommandent de le différer. A ce jour, aucune étude n’a permis de comparer les taux
de morbidité et de mortalité entre une gastropexie effectuée en urgence et une gastropexie effectuée de manière différée. Cependant, des études récentes, effectuées en médecine vétérinaire et humaine, semblent considérées que différer le geste chirurgical afin d’améliorer les conditions opératoires, apportent un meilleur taux de survie2, 3.
La réanimation médicale correspond au traitement de l’état de choc dont la composante principale est l’hypovolémie relative. Elle est basée sur l’administration d’O2, de fluides (cristalloïdes, colloïdes de synthèse et/ou hypertonique) et d’antalgiques. Le sondage gastrique qui permet la décompression de l’estomac est indispensable et fait partie intégrante de la réanimation. Une équipe a récemment montré l’intérêt pronostique des dosages répétés de la lactatémie. Les chiens dont la lactatémie avait diminué de 42,2 % avec la mise en place des soins de réanimation ont présenté un taux de survie de 100 %. A l’inverse, le groupe dont la lactatémie avait présenté une diminution inférieure à 42,2 % a présenté un taux de survie de 56 %4.
Le sondage gastrique doit être réalisé précocement afin de décomprimer l’estomac. Cette décompression est primordiale pour diminuer la pression appliquée sur la veine cave caudale et favoriser le retour veineux, reperfuser la paroi stomacale, améliorer la ventilation et traiter la douleur5. Suivant l’état clinique de l’animal, le sondage est réalisé avec ou sans anesthésie. Dans notre cas, l’état d’agitation de l’animal ne nous permettait pas d’effectuer cet acte sans tranquillisation et anesthésie générale. La sonde peut être remplacée par une sonde de pharyngostomie ou par une sonde naso-gastrique. Ceci permet d’éviter les récidives de dilatations de l’estomac. La réanimation médicale est alors prolongée et le geste chirurgical différé.
L’objectif d’une gastropexie est de produire une adhérence permanente entre l’antre pylorique et la paroi abdominale droite sans altérer la fonction gastrique. Il existe une grande variété de techniques laparotomiques (tube de gastropexie, gastropexie circumcostale, incisionnelle…). Récemment, plusieurs techniques chirurgicales laparoscopiques ont été expérimentées dans ce but. Elles possèdent tous les avantages de la coeliochirurgie : magnificence et apport de lumière, réduction du traumatisme tissulaire et de la douleur donc de la durée d’hospitalisation. Une conversion en laparotomie reste toujours possible. Des études expérimentales ont montré que la résistance à la tension de la pexie réalisée sous cœlioscopie, l’histologie de l’adhérence et les fonctions gastriques étaient comparables aux autres techniques chirurgicales laparotomiques6.
La technique de gastropexie réalisée ici est une application de celle décrite par Rawlings en 2002 pour la gastropexie préventive7,8. Elle est rapide et ne nécessite que peu de matériel. Les sutures sont réalisées à l’extérieur de l’abdomen ce qui permet un apprentissage plus accessible comparé aux autres techniques décrites uniquement intraabdominales9,10.
La morbidité et la douleur postopératoire sont réduites6.
En effet, 2 incisions de 1 et 3 cm sont pratiquées par rapport à une laparotomie classique avec une incision de 10-15 cm.
Lors de dilatation simple, comme dans ce cas, l’estomac est en position physiologique. La majorité de la paroi peut être visualisée à la recherche de zone de nécrose. La couleur, l’épaisseur, la présence d’ondes péristaltiques et le saignement sont évalués. En cas de torsion, le pylore est recherché en position dorsale droite et peut être saisi par la pince à préhension et replacé en position physiologique sous contrôle visuel. La rate et les artères spléniques sont inspectées. Une congestion splénique est classique et la rate doit revenir à une taille subnormale une fois la torsion traitée. La présence d’infarcissement de la paroi stomacale ou de thrombose des artères spléniques requiert un traitement chirurgical supplémentaire et l’intervention est convertie en laparotomie classique5.
En conclusion, lors de SDTE, la réanimation médicale a pour but de traiter l’état de choc et la compression de la veine cave caudale. Ceci permet de diminuer les risques anesthésiques et améliore le pronostic. La possibilité de laisser en place une sonde gastrique qui évite les récidives de dilatations autorise le différé de l’intervention chirurgicale tout en continuant la réanimation médicale et la surveillance des grandes fonctions.
Les techniques de gastropexie par laparoscopie sont applicables dans les cas de SDTE et donnent des résultats équivalents à la laparotomie. La morbidité post opératoire est réduite en raison de l’abord mini-invasif de la cavité abdominale. Lors de doute sur l’intégrité de la paroi stomacale ou d’une thrombose splénique, une conversion en laparotomie est réalisable rapidement.
Bibliographie
|
