L’hémostase en chirurgie
- “Tout saignement s’arrête” : même si cet idiome s’avère vrai dans tous les cas, nous disposons de nombreux moyens pour que ce saignement ne s’arrête pas par exsanguination de l’animal.
Auteur : Dr. S. Etchépareborde 13-06-2014 Centre Hospitalier Vétérinaire des Cordeliers, 29 avenue du Maréchal Joffre, 77100 Meaux. E-mail : setchepareborde@chvcordeliers.com Cet article a été publié dans : PratiqueVet (2014) 49 : p 249-253
Objectifs pédagogiques
Être capable de réaliser une hémostase de qualité durant une chirurgie.
Crédit de formation continue
La lecture de cet article ouvre droit à 0,05 CFC. La déclaration de lecture, individuelle et volontaire, est à effectuer auprès du CNVFCC.
L’hémostase en chirurgie
Une bonne hémostase est l’un des six principes fondamentaux de Halsted en chirurgie. Notre arsenal en ce but est large. Les moyens permettant de réduire le flux sanguin sont déjà largement utilisés dans toutes les cliniques (compression, bistouri électrique, ligatures) ou se démocratisent (fusion tissulaire, hémoclips). Une autre facette de l’hémostase est l’utilisation d’agents hémostatiques locaux et enfin les agents hémostatiques systémiques.
Une hémostase correcte améliore la visibilité, améliore la cicatrisation, diminue le risque d’œdème et d’infection et évite l’hypotension. Un animal vigile en bonne santé peut compenser une perte de 40 % de sa volémie avant de voir baisser ses pressions artérielles. Cette même perte chez un animal anesthésié est létale. En effet, une hémorragie grave non contrôlée conduit au choc, à l’hypothermie, à l’acidose, à la consommation des facteurs de coagulation et à l’hémodilution qui, à leur tour, entraînent une coagulopathie et accélèrent le saignement.
Le premier rôle d’une bonne hémostase est donc d’éviter la diminution des pressions sanguines. Une bonne hémostase permet également de conserver un champ opératoire propre et ainsi de s’assurer de la meilleure visibilité possible 1.
Cette visibilité est la garante d’un geste chirurgical précis permettant d’éviter au maximum les erreurs techniques. Enfin, une bonne hémostase diminue le risque d’hématomes, séromes et infections en période postopératoire.
Pour le cas particulier des chirurgies des cancers, elle évite la dissémination des cellules tumorales.
Il faut cependant garder à l’esprit que même la meilleure des hémostases ne pallie pas une coagulopathie préexistante. Avant toute chirurgie à risque (animal débilité, chirurgies hépatiques, chirurgies associées à des saignements incontournables type rhinotomie….), il est ainsi nécessaire d’effectuer un bilan de l’hémostase (temps de saignement muqueux, temps de coagulation, numération plaquettaire).
Il existe plusieurs moyens physiques pour réaliser l’hémostase
La compression
Une artère coupée se contracte jusqu’à 35 % de son diamètre initial grâce à sa musculature lisse. Ce phénomène est moins important pour les veines. Arrêter le flux sanguin en pressant à l’aide d’une compresse ou à l’aide d’un clamp favorise la mise en place du clou plaquettaire. Celui-ci se met en place en 30 secondes puis est consolidé par le réseau de fibrine en 2 à 3 minutes 2.
Cette durée dépend du diamètre du vaisseau, de la pression sanguine et de la coagulabilité. Ce clou plaquettaire reste néanmoins fragile et il faudra veiller à ne pas l’arracher en enlevant la compresse.
Il faut également éviter de frotter une plaie avec une compresse pour nettoyer en fin de chirurgie car ce geste est non seulement traumatique pour les tissus mous (abrasion par la compresse) mais tend à arracher les clous plaquettaires et augmente le risque de saignement.
Pour les vaisseaux de plus grand diamètre, la compression permet de diminuer le saignement de manière temporaire avant de réaliser une hémostase plus définitive. Si le vaisseau est comprimé à l’aide d’un clamp, on peut le bistourner avant de relâcher le clamp.
Les ligatures
Quelle que soit la taille du vaisseau, le ligaturer est toujours valable. Pour les veines, une simple ligature suffit. En revanche, pour les artères d’une taille raisonnable (plus de 2 mm de diamètre), il est conseillé de réaliser une ligature transfixiante protégée en amont par une ligature simple. Pour les ligatures, un fil tressé résorbable (polyglactin 910) apportera la meilleure tenue du nœud. Un monofilament reste cependant tout à fait acceptable et est même recommandé pour la réalisation d’une ligature transfixiante. Une aiguille ronde est alors utilisée. Toute ligature est entamée avec un nœud de chirurgien, sécurisé par 3 nœuds simples. La taille de suture la plus appropriée est du 3-0 (2 metric) et représente le meilleur compromis entre la solidité de la ligature et la tenue du nœud qui est inversement proportionnelle au diamètre du fil.
Les hémoclips
À la place des ligatures, des hémoclips peuvent être utilisés (Photo 1). Ils ont l’avantage d’être posés rapidement, peuvent être mis dans des sites difficiles à atteindre (lésion de l’artère glutéale caudale dans le cas de hernie périnéale, saignement autour d’une glande surrénale, saignement de l’artère linguale dans une chirurgie de sialocèle,…) et ne provoquent pas de dégâts sur les tissus adjacents comme le ferait le bistouri électrique. Les plus grands peuvent obturer des vaisseaux de 11 mm de diamètre. Leur principal inconvénient est la sécurité dans la mesure où le clip peut avoir tendance à glisser. Le prix du clip pour les pinces automatiques est d’environ 5 euros et tombe à 1,50 euro pour les pinces manuelles.
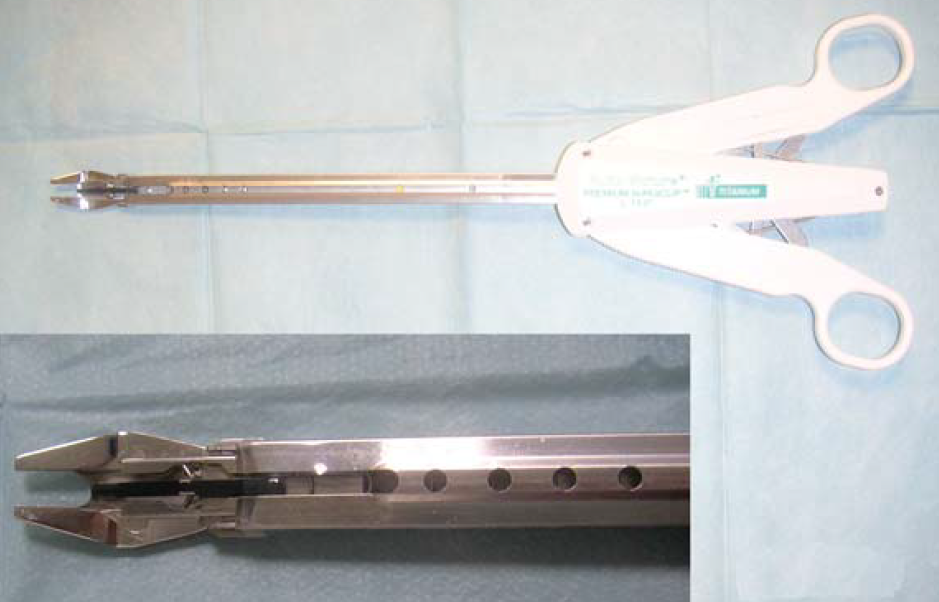
Photo 1 : Pince à hémoclips automatique. Avec ce type de pince à usage unique (mais pouvant être stérilisée à froid), la recharge d’hémoclips se trouve dans le manche et dès qu’un clip est posé un nouveau clip est présenté. Il existe des pinces manuelles, disponibles dans toutes les centrales, qui réalisent le même travail.
L’électrochirurgie
Le bistouri électrique
Il induit un courant électrique qui déshydrate les cellules et coagule les vaisseaux.
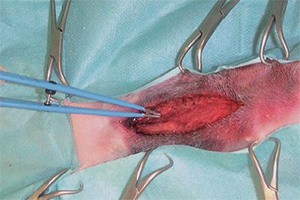
- Avec un bistouri monopolaire, l’animal en entier fait partie du circuit électrique et le courant généré par le bistouri passe du bistouri à une électrode placée sous l’animal. Il est très important que le contact entre le chien et l’électrode soit le plus grand possible pour éviter le risque de brûlures (Photo 2).
- Dans le cas d’un bistouri bipolaire, qui se présente sous la forme d’une pince, le courant passe d’un mors à l’autre et a ainsi un cheminement beaucoup plus court dans l’animal (Photo 3). Le haut courant ainsi généré peut également être utilisé dans les tissus humides contrairement au bistouri monopolaire pour lequel le contact avec le liquide entraîne une dispersion du courant.
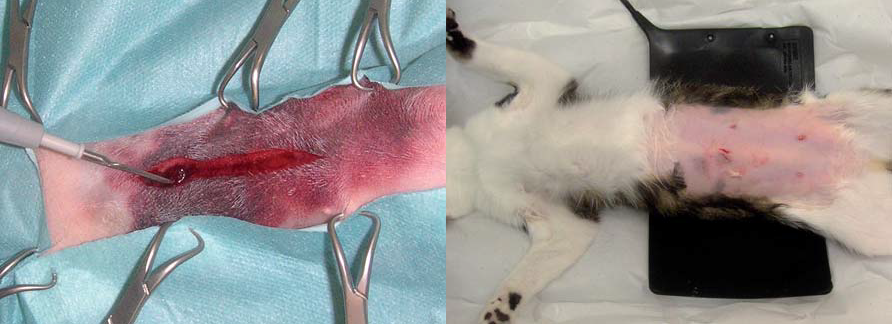
Photo 2 : Bistouri électrique monopolaire (en haut). Il peut être utilisé suivant deux modes : section (bouton jaune) et coagulation (bouton bleu). Il est très important que l’électrode (la plaque) soit bien en contact avec l’animal et que ce contact soit le plus large possible.
L’idéal est de la positionner sous une large zone tondue pour éviter toute interférence avec les poils qui sont isolants.
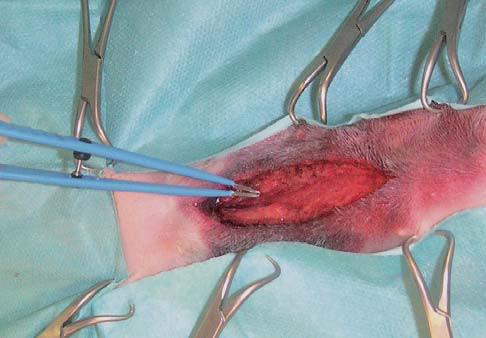
Photo 3 : Bistouri électrique bipolaire. Il se présente sous forme de pince. Le courant circule entre les deux mors et non plus à travers le chien.
Comparé à la lame froide, l’utilisation d’un bistouri électrique augmente le risque d’infection et retarde la cicatrisation : il faut donc évaluer la balance bénéfice (gain de temps chirurgical, moins de saignements)/risque (infection, cicatrisation) avant de l’utiliser.
La fusion tissulaire
L’utilisation de la fusion tissulaire se répand de plus en plus en médecine vétérinaire. Le principe est la combinaison d’un bistouri bipolaire avec une pression appliquée par les mâchoires de l’instrument 3.
La fusion tissulaire dénature le collagène et l’élastine des parois vasculaires qui se refusionnent pour obstruer le vaisseau. On peut ainsi coaguler des artères mesurant jusqu’à 7 mm de diamètre. Il existe des instruments pour la chirurgie ouverte et pour la chirurgie laparoscopique (Photo 4).
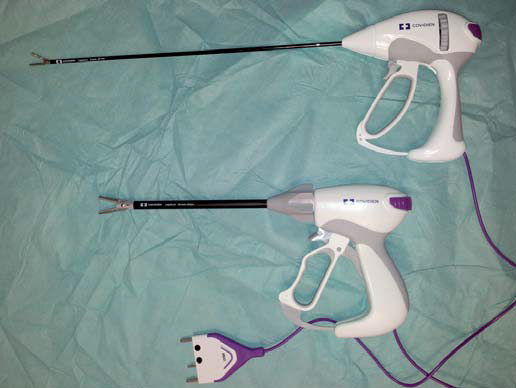
Photo 4 : Pinces de fusion tissulaire. Les pinces présentées ici permettent de coaguler les tissus et de les couper grâce à une lame glissant entre les mors. En bas, pince pour chirurgie ouverte et en haut pince pour chirurgie laparoscopique.
Le prix d’une pince à usage unique (mais pouvant être restérilisée à froid pour plusieurs dizaines d’utilisation) varie entre 250 et 500 euros suivant le modèle de la pince.
L’énergie par les ultrasons : le bistouri harmonique
Le bistouri utilisé décharge des vagues d’ultrason à une fréquence de 55,5 kHz. Les vibrations provoquées induisent un effet de “scie oscillante” tout en produisant de la chaleur et de la coagulation.
Ces bistouris ont l’avantage de couper et coaguler simultanément les tissus mous, les vaisseaux et les canaux lymphatiques. Ils travaillent à des températures plus basses que les lasers ou l’électrochirurgie. Ainsi, il n’y a quasiment aucune carbonisation des tissus ni de phénomène d’adhérence du tissu coagulé avec l’instrument. Ceci réduit les fumées ou la vapeur et améliore ainsi la visibilité.
Les lasers
L’outil utilisé projette des photons sur le tissu traité. Il s’en suit une interaction qui dépend, d’une part de la longueur d’onde du photon émis, et d’autre part des propriétés du tissu à couper.
Il existe de nombreux lasers différents, chacun possédant sa propre longueur d’onde qui est elle-même intimement liée à la profondeur de coupe du laser. Le laser peut être utilisé pour couper, cautériser, coaguler ou vaporiser.
La production de chaleur peut être importante et dépend des caractéristiques du laser, des tissus traités (proportion d’eau, couleur) et de l’environnement (gazeux ou liquide).
Les lasers peuvent être dangereux pour les yeux et les autres tissus et des précautions doivent être prises lors de son utilisation.
L’occlusion à distance
Le procédé le plus répandu pour cette pratique est l’utilisation d’un garrot. Cela concerne toutes les chirurgies distales au carpe ou au tarse ou de la queue. Il est recommandé d’utiliser des garrots plats vendus dans les centrales.
En effet, l’utilisation de simples liens ou de garrots étroits concentre la pression du garrot sur une zone très étroite et, de ce fait, est très traumatique. Il faut veiller à ne pas laisser un garrot en place trop longtemps. Aucune donnée vétérinaire ne mentionne la durée maximale de pose d’un garrot. La plupart des recommandations mentionnent une durée maximale de 90 minutes à 2 heures 1.
Le principal inconvénient est de laisser des vaisseaux non ligaturés dans le site chirurgical.
Il faut également se méfier de la vasodilatation et de l’hypotension induites par le relâchement du garrot en relation avec le relargage de l’acide lactique et du potassium concentrés dans le membre traité.
Une autre façon de faire est l’occlusion directe du vaisseau irriguant la zone à opérer : par exemple occlusion de l’artère carotide lors de chirurgie invasive de la mâchoire ou occlusion de la veine cave lors de surrénalectomie avec embole vasculaire.
Les vaisseaux sont occlus temporairement avec un clamp bulldog ou un tourniquet (Photo 5).
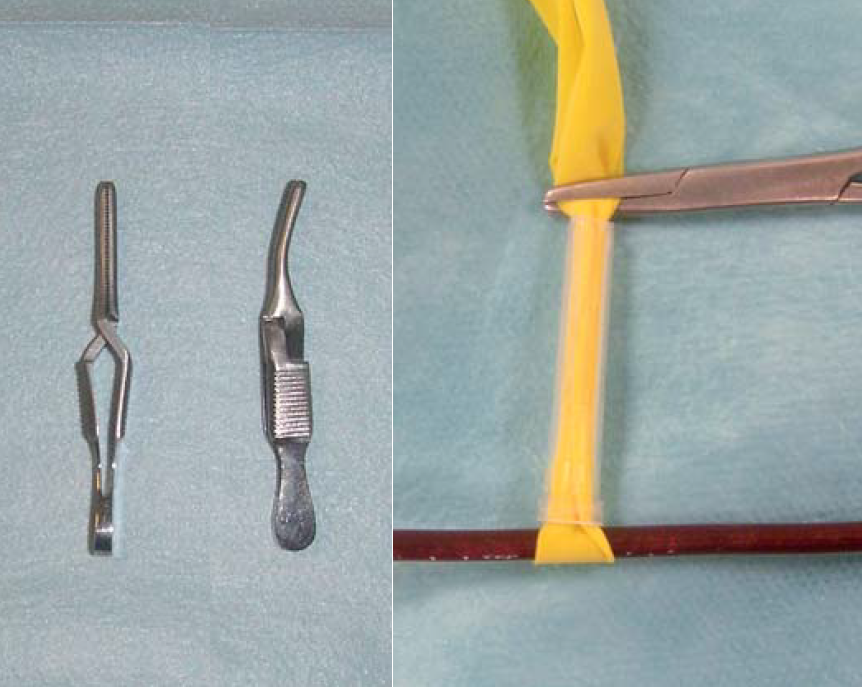
Photo 5 : À gauche, clamps bulldog. Ils peuvent être appliqués directement sur le vaisseau à occlure. À droite, représentation d’un tourniquet : un drain de Penrose (ou une bande de nylon) est passé autour du vaisseau puis le drain est passé à l’intérieur d’un capuchon d’aiguille (dont l’extrémité a été coupée). On occlut ensuite le vaisseau en tirant sur le drain de Penrose et l’on maintient la tension à l’aide d’un clamp comme illustré sur la photo.
La voie locale crée une barrière mécanique
Mise à part l’eau décrite dans ce paragraphe, les agents hémostatiques locaux visent à absorber le sang et permettent une barrière mécanique au saignement. Certains créent une matrice favorisant la formation du clou plaquettaire. Ils sont tous résorbables et peuvent être laissés dans la plaie. On utilise principalement ces agents lors des saignements diffus (chirurgie du foie) ou lorsque le vaisseau qui saigne se trouve dans une zone non accessible (sinus veineux vertébral).
L’eau glacée
Le froid entraînant une vasoconstriction, l’eau glacée reste une aide précieuse dans les zones où il est impossible de coaguler tous les points de saignement comme les chirurgies nasales qui sont sa principale indication. Son usage est proscrit dans l’abdomen car il entraînerait une hypothermie trop marquée. Pour réaliser ce type d’hémostase, une poche de NaCl ou de Ringer lactate stérile est mise au congélateur avant la chirurgie en prévision.
De l’adrénaline peut être ajoutée à l’eau à la dose de 1/1000 à 1/100 000 U/mL 4. L’adrénaline entraîne une puissante vasoconstriction. Son principal inconvénient est le risque de vasoconstriction systémique car elle est absorbée par les muqueuses. L’adrénaline peut aussi entraîner des arythmies et son utilisation doit se faire sous contrôle ECG.
Les éponges de gélatine
(Gelfoam®[H], Surgifoam®[H])
Au contact du sang, ces dispositifs gonflent et créent une matrice pour le réseau de fibrine qui va stabiliser le clou plaquettaire. Les études expérimentales montrent une résorption en 5 semaines environ. Ces éponges sont peu chères et se conservent longtemps à température ambiante.
Les éponges de collagène
(Ultrafoam®[H], Instat®[H], Pangen®[H])
Une étude a montré qu’elles seraient le meilleur agent hémostatique devant les éponges de gélatine puis la cellulose 5. Contrairement aux éponges de gélatines, elles favorisent l’agrégation plaquettaire en améliorant l’activation des plaquettes et en accélérant la formation du clou plaquettaire.
Le collagène est absorbé par les fibroblastes en 8 à 10 semaines. Tout comme les éponges de gélatine, elles peuvent être le support d’infection, provoquer des réactions de rejet et entraîner des gonflements (Photo 6).

Photo 6 : Une éponge de collagène est ici prédécoupée afin d’être utilisée pour des biopsies de foie.
La cellulose
(Surgicel®[H])
Sous forme de compresse, la cellulose forme un gel obstruant les saignements. Selon une étude, c’est le moins efficace des agents hémostatiques 5.
Son principal avantage est son effet bactéricide. La cellulose est absorbée en 2 à 6 semaines. Néanmoins, un cas de granulome inflammatoire a été décrit plusieurs années après son implantation et lorsqu’elle est utilisée pour les chirurgies de la moelle, il est recommandé de la retirer dès que l’hémostase est obtenue 6.
La cire à os
(Bone wax®[H], Ostene®[H])
La cire à os est un mélange de cire d’abeille et de paraffine (Photo 7). Elle est appliquée par pression sur un os qui saigne (mandibulectomie, sternotomie) et joue un rôle purement mécanique pour empêcher les saignements. Certaines études décrivent des réactions sur corps étranger ou une augmentation du risque d’infection ainsi qu’une gêne à la cicatrisation osseuse 7. Par précaution, on évite donc son utilisation dans les chirurgies contaminées ou lorsqu’une cicatrisation rapide est indispensable.
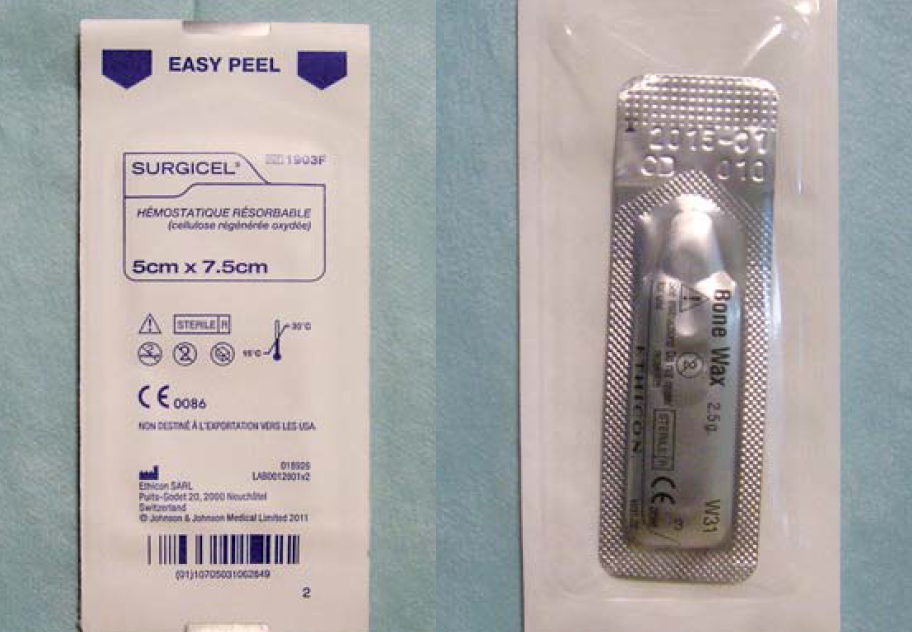
Photo 7 : Présentation des compresses hémostatiques de cellulose (à gauche) et de cire à os (à droite). Le temps de conservation est long et ces produits se stockent à température ambiante.
La voie systémique est peu utilisée
La desmopressine
C’est un analogue synthétique de la vasopressine arginine qui stimule la libération du facteur VIII et du facteur de von Willebrand. Aucun effet positif n’est décrit chez un animal sain. Elle est donc utilisée pour traiter les animaux déficients en facteur de von Willebrand (fréquemment les Dobermanns) 8. Le principal effet secondaire est un effet antidiurétique.
L’étamsylate
(Hemoced®[H])
Il peut être administré par voie orale ou injectable. Son action supposée est d’améliorer l’agrégation plaquettaire en cas de dégâts vasculaires 9. Sa toxicité est faible et les chiens et les chats supportent des doses jusqu’à 200 mg/kg. La liste des agents hémostatiques présentés ici n’est pas exhaustive mais représente les principaux moyens utilisés couramment en médecine vétérinaire et dont l’approvisionnement est aisé.
D’autres molécules sont utilisées en médecine humaine mais n’ont pour l’instant qu’un intérêt expérimental chez le Chien ou le Chat.
La disposition de tous ces moyens permet de s’adapter à la situation et d’agir vite en cas de saignement important ou de localisation difficile. Néanmoins, aucun n’est indispensable et rien ne remplace la bonne utilisation d’un clamp hémostatique et la sécurité d’une simple ou double ligature quand cela est possible.
Points forts
|
À lire…
|